Führen Sie ein normales Leben mit moderner Behandlung bei Morbus Crohn (CED)
Leben mit einer chronisch entzündlichen Darmerkrankung
Bei Morbus Crohn und anderen chronisch entzündlichen Darmerkrankungen (CED) wie Colitis ulcerosa steht für viele Betroffene eine Frage im Zentrum: Kann ich ein möglichst normales Leben führen? Unsere Antwort bei Vivomed – Gastroenterologie Bern:
Mit einer frühzeitigen Diagnose, modernen, leitlinienbasierten Therapien und einer engmaschigen Betreuung ist das in den meisten Fällen möglich.
Was ist Morbus Crohn?
Morbus Crohn ist eine chronische, meist schubweise verlaufende transmurale Entzündung des Verdauungstraktes. Typisch betroffen sind:
- das terminale Ileum (letzter Abschnitt des Dünndarms)
- der Dickdarm (Kolon)
Grundsätzlich kann aber jeder Abschnitt vom Mund bis zum After erkranken. Die Entzündung ist transmural, das heisst, sie betrifft alle Wandschichten des Darms und kann dadurch zu Engstellen (Stenosen), Fisteln und Abszessen führen.
Morbus Crohn gehört zu den CED und ist auch unter den Bezeichnungen regionale Enteritis, granulomatöse Ileitis oder Ileokolitis bekannt.
Typische Symptome bei Morbus Crohn
Nicht alle Patientinnen und Patienten haben die gleichen Beschwerden. Häufige Zeichen eines Schubs sind:
- Chronische Durchfälle (oft ohne viel Blut)
- Bauchschmerzen und krampfartige Beschwerden
- Gewichtsverlust
- Appetitlosigkeit
- Müdigkeit
- Fieber und allgemeines Krankheitsgefühl
- Perianale Beschwerden wie Fissuren, Fisteln oder Abszesse im Analbereich
- Zusätzlich können extraintestinale Manifestationen auftreten, also Beschwerden ausserhalb des Darms, z. B.:
- Gelenkentzündungen und -schmerzen (Arthritis, Arthralgie)
- Hautveränderungen (z. B. Erythema nodosum, Pyoderma gangraenosum)
- Augenentzündungen (Uveitis, Iritis, Episcleritis)
- Leber- und Gallenwegserkrankungen (z. B. primär sklerosierende Cholangitis)
- Wachstumsstörungen und Anämie bei Kindern und Jugendlichen
Gerade bei Kindern können Allgemeinsymptome wie Fieber, Blutarmut oder Wachstumsverzögerung im Vordergrund stehen – auch wenn Bauchschmerzen und Durchfall nicht stark ausgeprägt sind.
Wie wird Morbus Crohn diagnostiziert?
Morbus Crohn wird klinisch diagnostiziert – es gibt kein einzelnes „Crohn-Labor“ oder eine einzelne „Crohn-Untersuchung“. Typischerweise kombinieren wir:
- Gespräch & körperliche Untersuchung
Ausführliche Anamnese (Beschwerden, Dauer, familiäre Belastung, Rauchen, Medikamente)
Körperliche Untersuchung, Beurteilung von Bauch, Anus, Gelenken, Haut etc. - Labor und Stuhluntersuchungen
Entzündungswerte (z. B. CRP, BSG), Blutbild, Eisenstatus, Vitamin B12, Vitamin D, Albumin - Stuhltests auf Darmkeime wie Clostridioides difficile
- Fäkales Calprotectin (FC) zur Unterscheidung entzündlicher vs. nichtentzündlicher Ursachen des Durchfalls
- Endoskopie (Spiegelungen)
- Ileokoloskopie (Dickdarmspiegelung mit Darstellung des terminalen Ileums): Entnahme von Biopsien aus befallenem und unauffälligem Gewebe, Dokumentation von Ausdehnung und Schweregrad
- Ösophago-Gastro-Duodenoskopie (ÖGD) bei Beschwerden im oberen Verdauungstrakt
- Bildgebung
- MR- oder CT-Enterographie zur Darstellung des Dünndarms, von Stenosen, Fisteln und Abszessen
- Intestinaler Ultraschall (IUS) als strahlungsfreie, wiederholbare Methode zur Kontrolle der Entzündung
- MRT des Beckens oder Endosonographie bei perianalen Fisteln
- Bei Verdacht auf Abszess oder komplizierten Verlauf: CT/MR Abdomen & Becken
Wie kann Morbus Crohn unbehandelt verlaufen?
Morbus Crohn beginnt mit einer entzündlichen Reaktion der Krypten und mit Kryptenabszessen, die zu kleinen fokalen aphthoiden Ulzera fortschreiten. Diese Schleimhautschäden können sich zu tiefen longitudinalen und transversalen Ulzera mit dazwischenliegendem Schleimhautödem weiterentwickeln und auf diese Weise das charakteristische Bild eines Pflastersteinreliefs hervorrufen.
Die transmurale Ausbreitung der Entzündung führt zu einem Lymphödem und zu einer Verdickung der Darmwand und des Mesenteriums. Das mesenterische Fett weitet sich typischerweise auf die Serosaoberfläche des Darms aus. Die mesenterialen Lymphknoten sind häufig vergrößert. Die ausgeprägte Entzündungsreaktion kann zur Hypertrophie der Musculares mucosae, Fibrose und zu Strikturbildungen und damit zum Darmverschluss führen.
Abszesse treten häufig auf, Fisteln penetrieren oft in die anliegenden Strukturen, inkl. anderer Darmschlingen, der Blase oder des M. psoas. Fisteln können sich auch bis in die Haut am vorderen Abdomen oder in die Flanken erstrecken. Unabhängig von der intraabdominalen Krankheitsaktivität treten perianale Fisteln und Abszesse in 25–33% der Fälle auf und stellen häufig die lästigsten Komplikationen beim Morbus Crohn dar.
Nichtverkäsende Granulome können in den Lymphknoten, im Peritoneum, in der Leber und allen Schichten der Darmwand vorkommen. Obwohl ihr Vorliegen pathognomonisch ist, werden sie bei etwa der Hälfte der Patienten mit einem Morbus Crohn nicht gefunden. Das Vorkommen von Granulomen scheint mit dem klinischen Verlauf der Krankheit nicht in Verbindung zu stehen.
Die Segmente des erkrankten Darms sind vom benachbarten normalen Darm scharf demarkiert (sog. skip areas), daher der Name regionale Enteritis.
- Etwa 35% der Morbus-Crohn-Fälle betreffen das Ileum allein (Ileitis).
- Etwa 45% umfassen Ileum und Colon (Ileocolitis), mit einer Vorliebe für die rechte Seite des Dickdarms.
- Etwa 20% betreffen den Darm allein (granulomatöse Kolitis), von denen die meisten, im Gegensatz zu Colitis ulcerosa das Rektum aussparen.
Gelegentlich ist der gesamte Dünndarm betroffen (Jejunoileitis). Magen, Zwölffingerdarm oder Ösophagus sind klinisch nur selten betroffen, obwohl oft ein mikroskopischer Nachweis der Krankheit im Magenantrum gelingt, vor allem bei jüngeren Patienten. Wenn keine chirurgischen Maßnahmen durchgeführt werden, breitet sich die Krankheit beinahe nie auf Regionen des Dünndarms aus, die bei der Erstdiagnose nicht befallen waren.
Morbus Crohn & andere CED: Wer ist betroffen?
Morbus Crohn kann in jedem Alter auftreten, zeigt aber Häufungen im Alter von 17-40 Jahre. Viele Patientinnen und Patienten sind im jungen Erwachsenenalter, wenn die Erkrankung diagnostiziert wird – eine Lebensphase, in der Ausbildung, Beruf und Familienplanung eine wichtige Rolle spielen. Umso wichtiger ist eine gute, vorausschauende Therapieplanung.
Wie wird Morbus Crohn klassifiziert?
1. Morbus Crohn ist in drei prinzipielle Muster eingeteilt:
- in erster Linie entzündliche Form, die nach einem Verlauf von mehreren Jahren in der Regel in
- die v. a. stenotische oder obstruierende Form oder
- in die v. a. penetrierende oder fistelbildende Form übergeht.
Diese verschiedenen klinischen Muster erfordern unterschiedliche therapeutische Ansätze. Es gibt genetische Daten, die auf eine molekulare Basis dieser Klassifikation hinweisen.
2. Die Montreal Klassifikation klassifiziert M. Crohn wie folgt:
Manifestationsalter
- A1: < 16 Jahre
- A2: 17-40 Jahre
- A3: > 40 Jahre
Lokalisation
- L1: Ileum (Krummdarm; Teil des Dünndarms)
- L2: Kolon (Dickdarm)
- L3: Ileokolisch
- L4: Oberer Gastrointestinaltrakt (Magen-Darm-Trakt)
Biologisches Verhalten
- B1: nicht strikturierend, nicht penetrierend
- B2: strukturierend
- B3: intern penetrierend
- B4: perianal-penetrierend
Diese Einteilung hilft uns, das Risiko für Komplikationen (z. B. Stenosen, Fisteln, Operationen) einzuschätzen und die Therapie frühzeitig entsprechend anzupassen.
Risikofaktoren für einen aggressiven Verlauf sind z. B.:
- junges Alter bei Diagnose
- ausgedehnter Befall, v. a. Ileum/Ileokolon
- perianale/severe rektale Erkrankung
- ausgeprägte extraintestinale Manifestationen
- bereits penetrierendes oder strikturierendes Verhalten bei Diagnosestellung
3. Einteilung Schweregrad
Der Crohńs Disease Activity Index (CDAI) hilft den Schweregrad der Erkrankung im Verlauf zu erfassen. Dabei werden folgende Faktoren erfagt:
- Anzahl weicher Stühle
- Intensität der Bauchschmerzen
- Extraintestinale ("außerhalb des Darms") Manifestationen:
-
- Iritis (Regenhautentzündung)/Uveitis (Entzündung der mittleren Augenhaut, die aus der Aderhaut (Choroidea), dem Strahlenkörper (Corpus ciliare) und der Regenbogenhaut (Iris) besteht
- Stomatitis aphthosa ("Mundfäule")
- Pyoderma gangraenosum (PG; Synonym: Dermatitis ulcerosa) – sterile, destruierende, neutrophilenreiche und schmerzhafte Entzündung der Haut, bei der es großflächig, in der Regel an einer Stelle, zu einer Ulzeration (Geschwürbildung) und zu einem Gangrän (Gewebsuntergang aufgrund einer Ischämie oder sonstiger Schädigung) kommt.Beachte: Bei einer Pyoderma gangraenosum wird in bis zu 50 Prozent der Fälle eine Assoziation mit einer Systemerkrankung beobachtet (chronisch-entzündliche Darmerkrankungen (CED), Paraproteinämien, myeloproliferative und rheumatologische Erkrankungen).
- Erythema nodosum (Synonyme: Knotenrose, Dermatitis contusiformis, Erythema contusiforme; Plural: Erythemata nodosa) – granulomatöse Entzündung der Subkutis (Unterhautfettgewebe), die auch als Pannikulitis bezeichnet wird, und eine schmerzhafte Knötchenbildung (rote bis blaurote Farbe; später bräunlich). Die darüber liegende Haut ist gerötet.Lokalisation: beide Unterschenkelstreckseiten, am Knie und den Sprunggelenken; seltener an den Armen oder dem Gesäß
- Arthralgie/Arthritis (Gelenkschmerzen/Gelenkentzündung)
- Analfissur/Analfisteln
- Andere Fisteln
- Temperatur > 37 °C
-
- Symptomatische Durchfallbehandlung
- Resistenz im Abdomen
- Hämatokrit (Anteil der Erythrozyten (rote Blutkörperchen) am Volumen des Blutes)
- Körpergewicht
- Allgemeinbefinden
Beim Harvey-Bradshaw-Index wird die Schwere der Symptome bei Morbus Crohn, einschließlich abdomineller Schmerzen, Durchfall, Bauchmassen und allgemeinem Wohlbefinden bewertet.
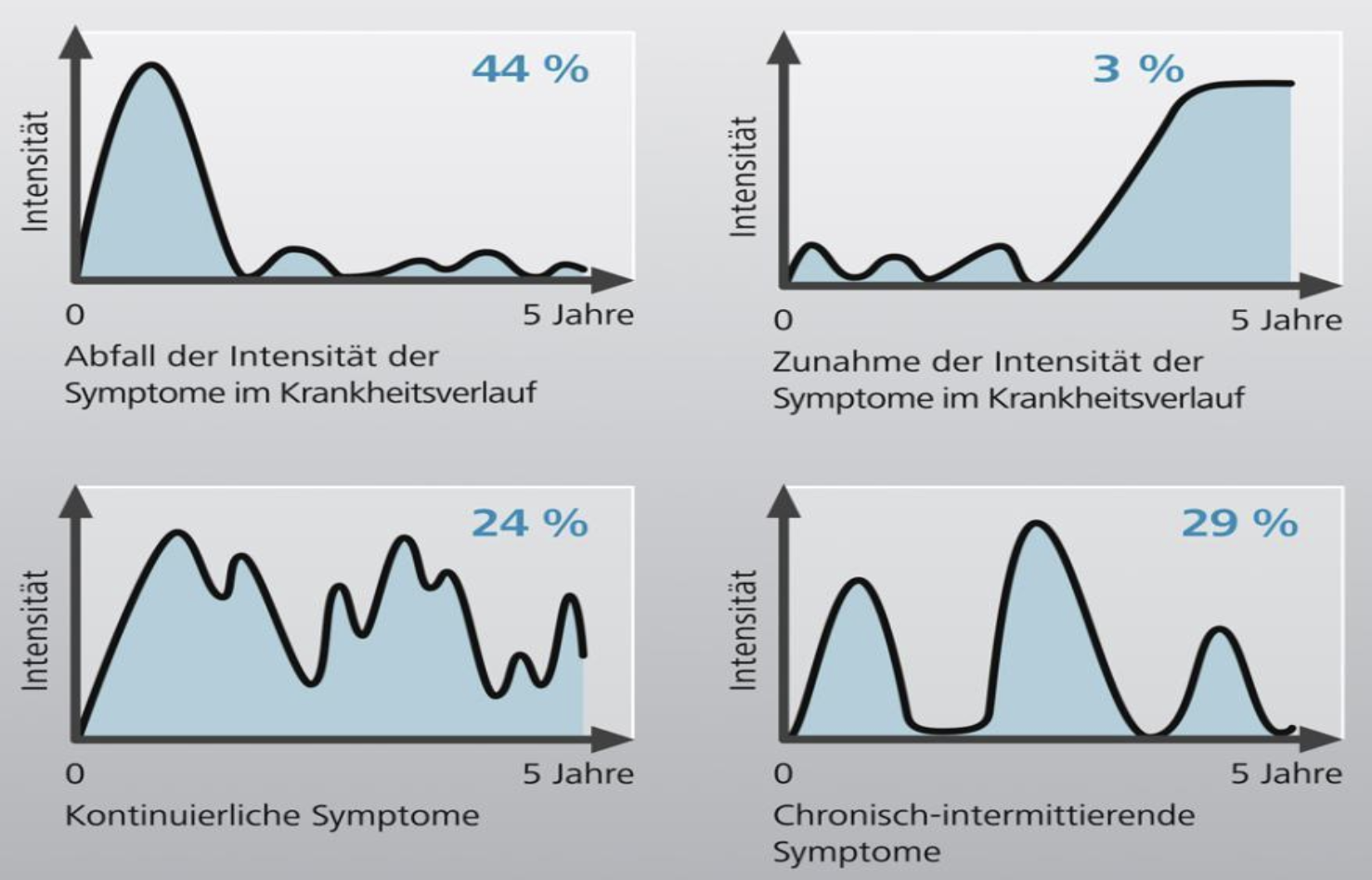
M. Henriksen et al., Scand J Gastroenterol. 2007; 42: 602-610
Komplikationen im Zusammenhang mit Morbus Crohn?
Bei den betroffenen Dünndarmsegmenten besteht ein erhöhtes Risiko für die Entwicklung von Karzinomen. Patienten mit Kolonbefall haben langfristig ein erhöhtes Risiko für kolorektale Karzinome, ähnlich wie bei Colitis ulcerosa, sofern die Krankheit in gleichem Ausmaß und für die gleiche Dauer besteht.
Chronische Malabsorption kann zu Nährstoffmängeln führen, insbesondere von Vitamin D und B12.
Das Toxische Megakolon ist eine seltene, aber ernste Komplikation von Colitis ulcerosa. Es handelt sich um ein klinisches Syndrom, das durch einen Ileus und eine koloniale Dilatation gekennzeichnet ist, die durch Röntgenaufnahmen nachgewiesen werden kann. Viele Fälle erfordern eine aggressive chirurgische Behandlung.
Symptome und Anzeichen von Morbus Crohn: Ein Überblick
Die häufigsten Symptome von Morbus Crohn umfassen:
- Chronische Diarrhö begleitet von Bauchschmerzen, Fieber, verminderter Appetit und Gewichtsverlust.Druckschmerz im Bauchbereich und möglicherweise eine tastbare Masse.Im Allgemeinen treten stärkere rektale Blutungen selten auf, es sei denn, es liegt ein isolierter Befall des Dickdarms vor, der ähnliche Symptome wie bei Colitis ulcerosa verursachen kann. Ein Drittel der Patienten leidet an perianalen Komplikationen wie Fissuren und Fisteln, die manchmal die dominierenden oder sogar initialen Beschwerden darstellen können.Bei Kindern treten häufig extraintestinale Manifestationen auf, darunter Arthritis, Fieber unklarer Herkunft, Anämie oder Wachstumsverzögerungen, auch wenn Bauchschmerzen und Durchfall nicht vorhanden sein müssen.
Die Symptome können bei Rückfällen der Krankheit variieren. Schmerzen sind häufig und können sowohl bei einfachen Rückfällen als auch bei komplizierenden Abszessen auftreten. Bei schweren Entzündungsschüben oder Abszessen zeigen Patienten oft eine ausgeprägte Empfindlichkeit, Schmerzen, Abwehrspannung und ein starkes Krankheitsgefühl. Stenotische Segmente können zu Darmverschlüssen führen, die sich durch Bauchkrämpfe, Blähungen, Verstopfung und Erbrechen äußern. Adhäsionen nach früheren Operationen können ebenfalls zu einem Darmverschluss führen, der oft plötzlich auftritt, ohne die üblichen Anzeichen wie Fieber, Schmerzen und allgemeines Unwohlsein, die typischerweise mit einem Verschluss aufgrund eines entzündlichen Schubs von Morbus Crohn einhergehen. Enterovesikale Fisteln können zu Blasenbildung im Urin (Pneumaturie) führen, während drainierende kutane Fisteln auftreten können. Eine freie Perforation in die Bauchhöhle ist selten.
Diese chronische Erkrankung kann auch eine Reihe von systemischen Symptomen verursachen, darunter Fieber, Gewichtsverlust, Mangelernährung und verschiedene extraintestinale Manifestationen.
Wie wird Morbus Crohn erkannt?
Der Verdacht auf einen Morbus Crohn stellt sich bei Patienten mit entzündlicher oder Verschlusssymptomatik oder bei Patienten ohne hervorstechende gastrointestinale Symptome, aber mit perianalen Fisteln oder Abszessen oder mit einer anderweitig nicht erklärbaren Arthritis, Erythema nodosum, Fieber, Anämie oder (bei Kindern) Wachstumshemmung. Eine positive Familienanamnese für Morbus Crohn erhöht den Verdacht.
Andere gastrointestinale Krankheiten, besonders Colitis ulcerosa können ähnliche Befunde und Symptome aufweisen (z. B. Bauchschmerzen, Diarrhö). Die Differenzialdiagnose der Colitis ulcerosa kann in den 20% der Fälle problematisch sein, in denen der Morbus Crohn auf das Kolon beschränkt ist. Da jedoch das therapeutische Vorgehen bei beiden ähnlich ist, bekommt die Unterscheidung nur dann Bedeutung, wenn ein operatives Vorgehen oder eine experimentelle Therapie in Erwägung gezogen werden.
Bei Patienten mit einem akuten Abdomen (entweder initial oder bei einem Rückfall) werden Abdomenübersichtsaufnahmen im Liegen und im Stehen und ein CT-Abdomen durchgeführt. Diese Untersuchungen zeigen Verschluss, Abszesse oder Fisteln und andere mögliche Ursachen eines akuten Abdomens (z. B. Appendizitis). Mithilfe des Ultraschalls kann eine gynäkologische Krankheit bei Frauen mit Beschwerden im unteren Abdomen und im Becken besser abgegrenzt werden.
Wenn die Krankheit weniger akut erscheint, kann eine Dünndarmdarstellung mit Zielaufnahmen des terminalen Ileums besser sein als eine konventionelle CT. Allerdings werden neuere Techniken der CT- oder MR-Enterographie/Enteroklyse, die hochauflösende CT- oder MR-Bildgebung mit Kontrastmittel kombinieren. Diese bildgebenden Verfahren sind nahezu diagnostisch, wenn sie charakteristische Stenosen oder Fisteln mit begleitender Separation von Darmschlingen zeigen.
Wenn die Befunde zweifelhaft sind, kann ein CT-Doppelkontrasteinlauf oder eine Videokapselenteroskopie oberflächliche Aphthen und lineare Ulzera anzeigen. Ein Bariumkontrasteinlauf kann angewendet werden, wenn die Symptome vorwiegend dem Dickdarm zugeordnet werden (z. B. Diarrhö), er kann den Reflux von Barium ins terminale Ileum mit Unregelmäßigkeiten, Knotigkeit, Steifheit, Wandverdickung und eingeengtem Lumen zeigen. Differenzialdiagnosen bei Patienten mit ähnlichen Röntgenbefunden umfassen Karzinome des Zäkums, ileales Karzinoid, Lymphom, systemische Vaskulitis, Bestrahlungsenteritis, ileozäkale Tuberkulose und Amöbom.
Bei atypischen oder unklaren Fällen (z. B. bei im Vordergrund stehender Diarrhö und nur minimalen Schmerzen) wird die Abklärung ähnlich wie bei Verdacht auf eine Colitis ulcerosa mittels Koloskopie durchgeführt (inkl. Biopsieentnahme, Probenentnahme für Darmpathogene und wenn möglich Einsicht in das terminale Ileum). Eine endoskopische Untersuchung des oberen Gastrointestinaltrakts (Oesophagogastroduodenoskopie (ÖGD)) kann eine subtile Beteiligung von Magen und Duodenum auch in solchen Fällen aufdecken, in denen keine Symptome eines Befalls des oberen Gastrointestinaltrakts bestehen.
Technische Untersuchungen für Morbus Crohn.
Labortests sollten auf Anämie, Hypoalbuminämie und Elektrolytstörungen untersuchen. Bei Patienten mit Kolonbefall könnten erhöhte Werte von alkalischer Phosphatase und Gamma-Glutamyltranspeptidase auf eine primär sklerosierende Cholangitis hinweisen. Leukozytose und erhöhte Spiegel von Akute-Phase-Proteinen wie Erythrozytensedimentationsrate und CRP können unspezifische Anzeichen sein, aber auch als Indikatoren für die Krankheitsaktivität dienen.
Um mögliche Mangelzustände zu erkennen, sollten Vitamin D- und B12-Werte alle 1–2 Jahre überprüft werden. Bei Verdacht auf Mangelzustände können zusätzliche Labortests für wasserlösliche Vitamine (Folsäure, Niacin), fettlösliche Vitamine (A, D, E, K) und Mineralien (Zink, Selen, Kupfer) durchgeführt werden.
Alle Patienten mit entzündlichen Darmerkrankungen sollten ihre Knochendichte überwachen lassen, üblicherweise durch eine Röntgendichtemessung (DXA).
Perinukleäre antineutrophile zytoplasmatische Antikörper sind bei 60–70% der Patienten mit Colitis ulcerosa vorhanden, jedoch nur bei 5–20% der Patienten mit Morbus Crohn. Anti-Saccharomyces cerevisiae-Antikörper sind relativ spezifisch für Morbus Crohn, obwohl sie nicht routinemäßig zur Diagnose verwendet werden. Weitere Antikörper wie Anti-OmpC und Anti-CBir1 sind verfügbar, aber ihr klinischer Nutzen ist unklar; einige Studien deuten darauf hin, dass hohe Titer dieser Antikörper eine ungünstige Prognose haben könnten.
Prognose bei Morbus Crohn: Ein Überblick
Morbus Crohn ist in der Regel nicht heilbar, aber durch periodische Schübe und Remissionen gekennzeichnet. Einige Patienten erleben schwere Krankheitsverläufe mit häufigen Schmerzepisoden, die sie stark belasten können.
Mit einer angemessenen medizinischen Therapie und gegebenenfalls chirurgischen Eingriffen können die meisten Patienten erfolgreich behandelt werden. Die krankheitsbedingte Sterblichkeitsrate ist sehr gering. Die häufigste krankheitsbedingte Todesursache ist gastrointestinaler Krebs, insbesondere Kolon- und Dünndarmkrebs. Thromboembolische Komplikationen, insbesondere während aktiver Krankheitsschübe, können ebenfalls tödlich sein. Etwa 10% der Personen mit Morbus Crohn und den damit verbundenen Komplikationen werden dauerhaft beeinträchtigt.
Therapie bei Morbus Crohn – ein Überblick
Die Behandlung wird individuell an Ihre Situation, Krankheitsausdehnung, Schweregrad, Vorbehandlungen und Lebensplanung angepasst. Grundsätzlich unterscheiden wir:
- Akuttherapie („Induktion“) – Schubbehandlung
- Erhaltungstherapie („Maintenance“) – Rückfallprophylaxe
1. Allgemeine Massnahmen
- Rauchen einstellen: Rauchen verschlechtert Morbus Crohn und erhöht das Rezidiv- und Operationsrisiko.
- Ernährung optimieren: Je nach Befund individuelle Ernährungsempfehlungen; bei Stenosen ggf. Anpassung der Kostform.
- Mangelzustände korrigieren: z. B. Eisen, Vitamin B12, Vitamin D, Folsäure, Spurenelemente.
- Knochendichtekontrolle (DXA): insbesondere bei Steroidtherapie und langfristiger Erkrankung.
- Psychische Gesundheit berücksichtigen: Stress, Depression und Angst können Schübe beeinflussen und sollten aktiv mitbehandelt werden.
2. Behandlung milder Verläufe
Bei mildem Morbus Crohn und geringem Risiko für Progression können folgende Strategien sinnvoll sein:
- Budesonid (kontrollierte Freisetzung, 9 mg/Tag) bei leicht bis mässig aktivem Ileozökalbefall zur Induktion einer Remission.
- Keine routinemässige Langzeittherapie mit Budesonid zur Remissionserhaltung.
- Begleitend: Ernährungstherapie, Monitoring (Symptome, Calprotectin, Bildgebung).
3. Behandlung moderater bis schwerer Verläufe
Bei mittel bis schwer aktiver Erkrankung kommen heute oft frühzeitig Biologika und small molecules zum Einsatz – nicht erst nach Ausschöpfen aller konventionellen Therapien.
Akuttherapie (Induktion):
- Systemische Kortikosteroide (z. B. Prednison, Budenofalk) für die kurzfristige Schubtherapie
Bei unzureichendem Ansprechen oder ungünstigen Risikoprofilen: - Anti-TNF-Antikörper:
- Infliximab (Remicade)
- Adalimumab (Humira)
- Certolizumab Pegol (Cimzia)
- Anti-Integrin-Therapie:
- Vedolizumab (Entyvio)
- Anti-Interleukin-12/23 bzw. Anti-IL-23-Antikörper:
- Ustekinumab (Stelara)
- Risankizumab (SKYRIZI)
- Guselkumab (Tremfya)
- JAK-Inhibitoren (small molecules):
- Upadacitinib (RINVOQ)
Erhaltungstherapie (Maintenance):
- Fortführung der Biologika oder small molecules in angepasster Dosierung
- ggf. Kombination mit Immunmodulatoren (z. B. Azathioprin, 6-Mercaptopurin, Methotrexat), insbesondere zur Reduktion der Antikörperbildung gegen bestimmte Biologika
- Azathioprin/6-MP oder Methotrexat nicht als alleinige Induktionstherapie bei schwerer Erkrankung, aber als Option zur Remissionserhaltung nach Steroidinduktion
Wichtig:
Systemische Kortikosteroide sind nicht als Langzeit-Erhaltungstherapie geeignet – sie erhöhen das Risiko für Osteoporose, Infektionen und andere Nebenwirkungen.
4. Fistulierender und strikturierender Morbus Crohn
Bei perianalen Fisteln und komplizierten Verläufen:
- Zuerst: Abszessdrainage und ggf. Seton-Anlage (chirurgische Entlastung)
- Ergänzend:
- Antibiotika (z. B. Metronidazol, Ciprofloxacin)
- Anti-TNF-Therapie (Infliximab, Adalimumab) – mit belegter Wirksamkeit bei perianalen Fisteln
- ggf. Vedolizumab, Ustekinumab oder Upadacitinib bei ausgewählten Verläufen
- Bei Stenosen:
- Abklärung, ob entzündlich oder fibrotisch dominiert
- Entzündliche Stenosen können auf Biologika/small molecules ansprechen
- Ausgeprägte fibrostenotische Stenosen erfordern häufig endoskopische Dilatation oder Operation
5. Chirurgische Therapie
Etwa 30–50 % der Patientinnen und Patienten benötigen im Verlauf mindestens einen operativen Eingriff. Typische Gründe:
- wiederholter oder hochgradiger Darmverschluss (Ileus)
- komplexe, nicht beherrschbare Fisteln oder Abszesse
- Verdacht auf oder Nachweis eines Karzinoms
Operationen können die Lebensqualität deutlich verbessern, heilen Morbus Crohn aber nicht. Ein erneuter Entzündungsrückfall im Bereich der Anastomose (Nahtstelle) ist möglich.
Daher ist nach Operationen:
- eine frühe endoskopische Kontrolle (6–12 Monate) und
- bei Risikofaktoren eine prophylaktische medikamentöse Therapie (z. B. Anti-TNF, Vedolizumab, Metronidazol, Thiopurine)
sinnvoll, um Rückfälle rechtzeitig zu erkennen und zu verhindern
Langfristige Risiken & Vorsorge
Patientinnen und Patienten mit langjährigem Morbus Crohn mit Kolonbefall haben ein erhöhtes Risiko für kolorektale Karzinome. Deshalb empfehlen wir:
- regelmässige koloskopische Vorsorgeuntersuchungen mit gezielten Biopsien
- individuelle Intervalle je nach Dauer, Ausdehnung und Entzündungsaktivität
Bei Dünndarmbefall ist das Risiko für Dünndarmkarzinome erhöht – hier ist eine sorgfältige klinische und bildgebende Kontrolle wichtig.
Ihr Vorteil bei Vivomed – Gastroenterologie Bern
Bei Vivomed verbinden wir:
- Aktuelle internationale Leitlinien mit
- denkbar schonenden, individuell zugeschnittenen Behandlungsstrategien
Unser Angebot für Patientinnen und Patienten mit Morbus Crohn und anderen CED:
- Detaillierte Abklärung von Symptomen und Risikoprofil
- Moderne Endoskopie (inkl. Ileokoloskopie) und Bildgebung
- Intestinaler Ultraschall für Verlaufskontrollen ohne Strahlenbelastung
- Therapieplanung mit Biologika und small molecules nach aktuellem Evidenzstand
- Enge Zusammenarbeit mit Chirurgie, Radiologie,
- Ernährungsberatung und Rheumatologie
- Langfristige Begleitung inkl. Vorsorge,
- Impfberatung und psychosozialer Unterstützung
Unser Ziel: Gemeinsam mit Ihnen einen Weg finden, der Ihre Erkrankung möglichst gut kontrolliert und Ihnen ein aktives, selbstbestimmtes Leben ermöglicht.
Wann sollten Sie ärztliche Hilfe suchen?
Bitte nehmen Sie rasch Kontakt auf, wenn Sie:
- anhaltenden oder zunehmenden Durchfall haben
- Blut im Stuhl bemerken
- unter starken Bauchschmerzen, Fieber oder Gewichtsverlust leiden
- neue perianale Beschwerden (Schwellung, Schmerz, Sekretion) bemerken
- als bekannte/r CED-Patient/in einen deutlichen Rückfall Ihrer Beschwerden erleben
Frühes Handeln kann Komplikationen verhindern und die Therapieergebnisse verbessern.
Fazit
Morbus Crohn kann herausfordernd sein, aber mit einer ganzheitlichen Herangehensweise und professioneller Betreuung lässt sich die Lebensqualität verbessern. Erfahren Sie hier mehr über bewährte Strategien zur Bewältigung von Morbus Crohn und nehmen Sie aktiv Einfluss auf Ihre Gesundheit.
Aktuelle Therapieempfehlungen für Biologika und small molecules (mittelschwerer bis schwerer Morbus Crohn).
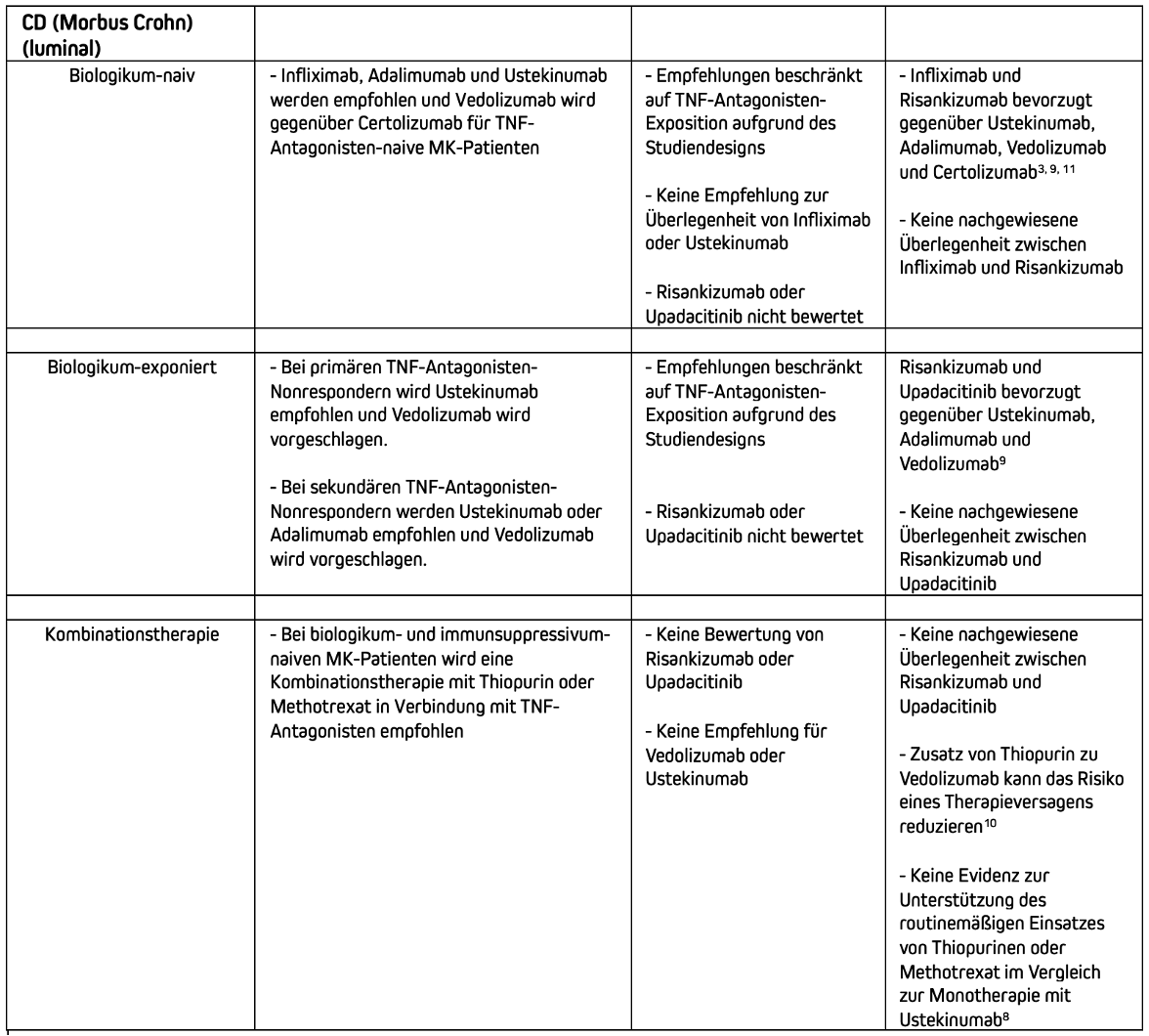
Therapieempfehlungen für Biologika und small molecules (mittelschwerer bis schwerer Morbus Crohn).
1. Sands BE, Peyrin-Biroulet L, Loftus EV Jr, et al. Vedoli-zumab versus adalimumab for moderate-to-severe ulcerative colitis. N Engl J Med 2019;381:1215-1226.
2. Narula N, Wong ECL, Marshall JK, et al. Comparative efficacy for infliximab vs vedolizumab in biologic naive ulcerative colitis. Clin Gastroenterol Hepatol 2022;20:1588-1597 e3.
3. Narula N, Wong ECL, Dulai PS, et al. Comparative effectiveness of biologics for endoscopic healing of the ileum and colon in Crohn's disease. Am J Gastroenterol 2022;117:1106-1117.
4. Lasa JS, Olivera PA, Danese S, et al. Efficacy and safety of biologics and small molecule drugs for patients with moderate-to-severe ulcerative colitis: a systematic review and network meta-analysis. Lancet Gastroenterol Hepatol 2022;7:161-170.
5. Burr NE, Gracie DJ, Black CJ, et al. Efficacy of biological therapies and small molecules in moderate to severe ulcerative colitis: systematic review and network meta-analysis. Gut 2022;71:1976-1987.
6. Kochhar GS, Desai A, Farraye FA, et al. Efficacy of bio-logic and small molecule agents as second-line therapy after exposure to TN inhibitors in patients with ulcerative colitis: a propensity-matched cohort study. Aliment Pharmacol Ther 2023;58:297-308.
7. Yzet C, Diouf M, Singh S, et al. No benefit of concomitant immunomodulator therapy on efficacy of biologics that are not tumor necrosis factor antagonists in patients with inflammatory bowel diseases: a meta-analysis. Clin Gastroenterol Hepatol 2021;19:668-679.
8.Hu A, Kotze PG, Burgevin A, et al. Combination therapy does not improve rate of clinical or endoscopic remission in patients with inflammatory bowel diseases treated with vedolizumab or ustekinumab. Clin Gastroenterol Hepatol 2021;19:1366-1376.
9. Barberio B, Gracie DJ, Black CJ, et al. Efficacy of biological therapies and small molecules in induction and maintenance of remission in luminal Crohn's disease: systematic review and network meta-analysis. Gut 2023; 72:264-274.
10. Kirchgesner J, Desai RJ, Schneeweiss MC, et al. Decreased risk of treatment failure with vedolizumab and thiopurines combined compared with vedolizumab mon-otherapy in Crohn's disease. Gut 2022;71:1781-1789.
11. Wong ECL, Dulai PS, Marshall JK, et al. Comparative efficacy of infliximao vs ustekinumab for maintenance of clinical response in biologic naïve Crohn's disease. Inflamm Bowel Dis 2023;29:1015-1023.